Der Login steht zurzeit nicht zur Verfügung.
Biosimilars: die wirtschaftliche und effektive Alternative zu Biologika
Biosimilars sind Nachahmerpräparate bereits zugelassener biologischer Arzneimittel, sogenannter Biologika. Biologika werden in der Versorgung immer wichtiger, sind aber auch sehr teuer. Die unabhängige Arzneimittelkommission der deutschen Ärzteschaft empfiehlt Biosimilars und deren Einsatz: Biosimilars sind bezüglich der therapeutischen Wirksamkeit, der Verträglichkeit und der Sicherheit in allen zugelassenen Indikationen dem jeweiligen Referenzarzneimittel gleichwertig und können wie diese eingesetzt werden. Detailinformationen erhalten Sie auf der Website der Arzneimittelkommission.
Vorteile von Biosimilars
- Biosimilars können dabei helfen, im Bereich der biologischen Arzneimittel wirtschaftlich zu verordnen.
- Biosimilars bieten die Chance einen Wettbewerb bei den teuren Biologika zu erzeugen, denn sie sind deutlich günstiger.
- Durch ihre Wirtschaftlichkeit tragen Biosimilars dazu bei, dass mehr Patienten eine Biologikatherapie erhalten können und somit eine Versorgungslücke geschlossen wird.
Wichtiger Hinweis zur Austauschbarkeit
Zum 15. März 2024 tritt mit dem §40b der Arzneimittelrichtlinie (AM-RL) nur teilweise eine Austauschbarkeit für Biosimilars in Kraft. Ab diesem Zeitpunkt muss bei der Herstellung einer parenteralen Zubereitung ein wirtschaftliches Produkt eingesetzt werden. Bei Fertigarzneimitteln wird weiterhin das namentlich verordnete Präparat an die Kunden abgegeben. Die Umstellung auf ein wirtschaftliches Biosimilar oder rabattiertes Produkt liegt ausschließlich in der Hand des verordnenden Arztes. Ausnahmen sind Bioidenticals, bei denen die Apothekerin oder der Apotheker eine Substitution vornehmen darf. Alle Biosimilars und Referenzprodukte finden Sie in Anlage VIIa der AM-RL auf der Seite des GBA.
Großes Potential durch wirtschaftliche Verordnungen
Durch Patentabläufe steigt die Verfügbarkeit von Biosimilars jährlich an, der Anteil an abgegebenen Biosimilars nimmt daher konstant zu und liegt bei ca. 25%. Durch das Mitwirken der Ärzteschaft können die Ausgaben der GKV nachhaltig gesenkt werden, wenn vorrangig Rabattvertragsartikel oder Biosimilars verordnet werden.
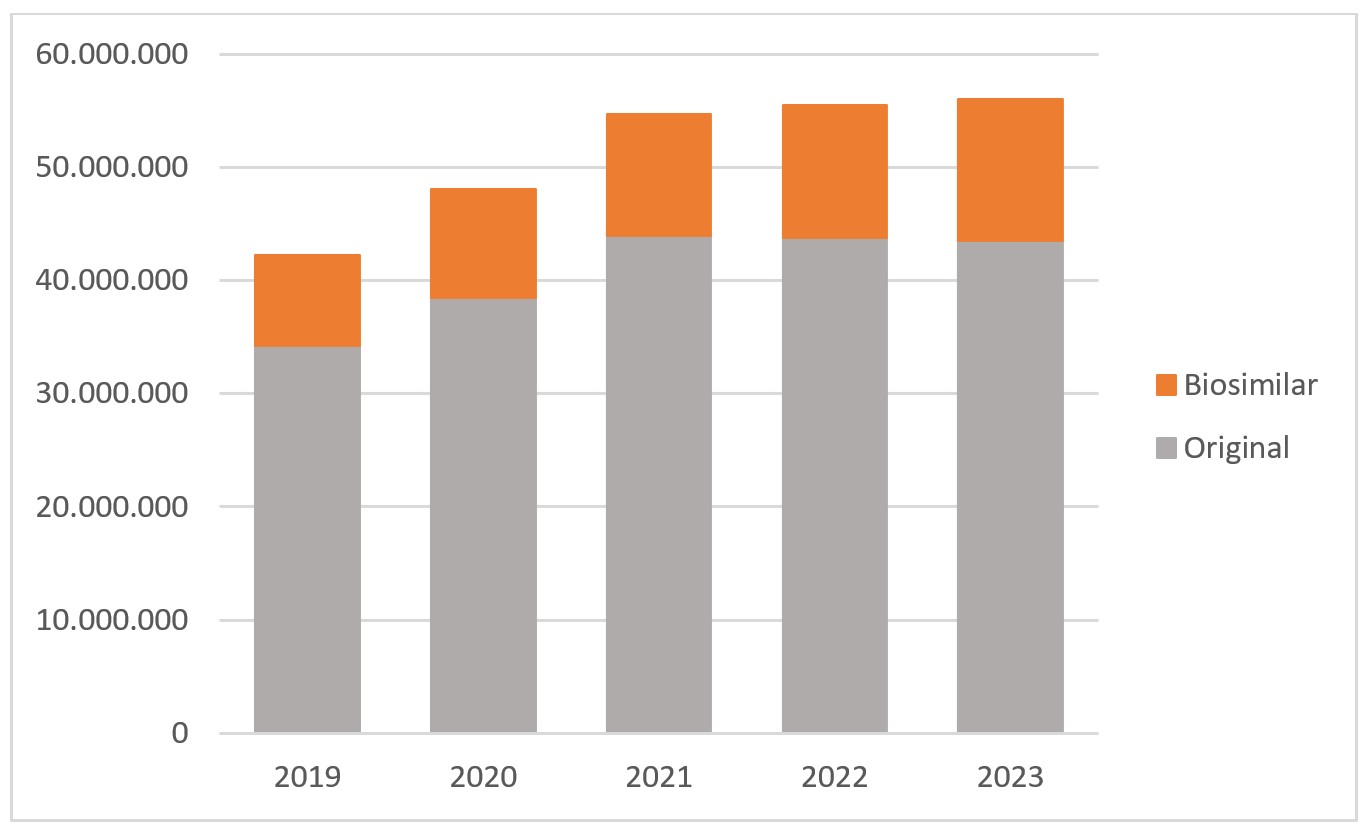 Abgegebene Tagesdosen (DDD) für Wirkstoffe mit verfügbaren Biosimilars
Abgegebene Tagesdosen (DDD) für Wirkstoffe mit verfügbaren Biosimilars
Preisvergleich* beispielhaft am Wirkstoff Rituximab
Rituximab | Kosten |
|---|---|
Referenzarzneimittel | ca. 2.170 Euro |
Biosimilar | ca. 1.693 Euro |
- 22 % |
* Nettokosten (AVP abzüglich gesetzliche Herstellerrabatte)
Unterschiede: Biosimilars, Generika, Bioidenticals
Biosimilars
Biosimilars sind Nachahmerpräparate bereits zugelassener biologischer Arzneimittel (Biologika). Sie ähneln dem Original in hohem Maße – sie dürfen nicht stärker von diesem abweichen als verschiedene Chargen des Originalprodukts selbst und sind somit therapeutisch gleichwertig. Für die Zulassung von Biosimilars gelten höhere Anforderungen als für Generika.
Bioidenticals
Bioidenticals sind biologische Arzneimittel, die im gleichen Prozess vom gleichen Hersteller produziert werden, aber unter verschiedenen Namen – von unterschiedlichen Pharmaunternehmen vermarktet – erhältlich sind. Die Arzneimittel selbst sind identisch.
Generika
Generika sind chemisch synthetisierte Nachahmerpräparate mit erprobten, patentfreien Wirkstoffen, die sich über einen langen Zeitraum therapeutisch bewährt haben. Die Wirkstoffe sind identisch, aber Hilfsstoffe und Herstellungsverfahren dürfen vom Original abweichen. Für die Zulassung sind keine eigenen Studien vorgeschrieben. Das macht Generika deutlich günstiger als die Erstanbieter.